Page 51 - NEWSLETTER_26
P. 51
ΑΡΘΡΟ
Απαλουταμίδη
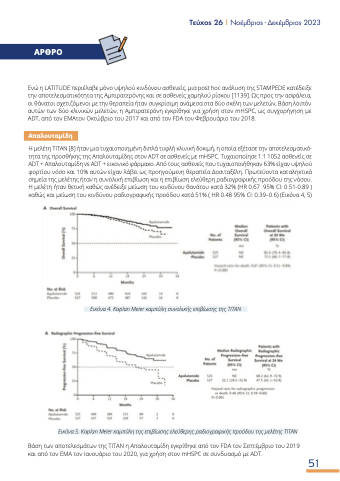
Εικόνα 4. Kaplan Meier καμπύλη συνολικής επιβίωσης της TITAN
Εικόνα 5. Kaplan Meier καμπύλη της επιβίωσης ελεύθερης ραδιογραφικής προόδου της μελέτης TITAN
Tεύχος 26 | Nοέμβριος - Δεκέμβριος 2023
Ενώ η LATITUDE περιέλαβε μόνο υψηλού κινδύνου ασθενείς, μια post hoc ανάλυση της STAMPEDE κατέδειξε την αποτελεσματικότητα της Αμπιρατερόνης και σε ασθενείς χαμηλού ρίσκου [1139]. Ως προς την ασφάλεια, οι θάνατοι σχετιζόμενοι με την θεραπεία ήταν συγκρίσιμη ανάμεσα στα δύο σκέλη των μελετών, Βάση λοιπόν αυτών των δύο κλινικών μελετών, η Αμπιρατερόνη εγκρίθηκε για χρήση στον mHSPC, ως συγχορήγηση με ADT, από τον EMAτον Οκτώβριο του 2017 και από τον FDA τον Φεβρουάριο του 2018.
Η μελέτη TITAN [8] ήταν μια τυχαιοποιημένη διπλά τυφλή κλινική δοκιμή, η οποία εξέτασε την αποτελεσματικό- τητα της προσθήκης της Απαλουταμίδης στον ADT σε ασθενείς με mHSPC. Τυχαιοποίησε 1:1 1052 ασθενείς σε ADT + Απαλουταμίδη vs ADT + εικονικό φάρμακο. Από τους ασθενείς που τυχαιοποιήθηκαν 63% είχαν υψηλού φορτίου νόσο και 10% αυτών είχαν λάβει ως προηγούμενη θεραπεία Δοσιταξέλη. Πρωτεύοντα καταληκτικά σημεία της μελέτης ήταν η συνολική επιβίωση και η επιβίωση ελεύθερη ραδιογραφικής προόδου της νόσου. Η μελέτη ήταν θετική καθώς ανέδειξε μείωση του κινδύνου θανάτου κατά 32% (HR 0.67 95% CI: 0.51-0.89 ) καθώς και μείωση του κινδύνου ραδιογραφικής προόδου κατά 51% ( HR 0.48 95% CI: 0.39–0.6) (Εικόνα 4, 5)
Βάση των αποτελεσμάτων της TITAN η Απαλουταμίδη εγκρίθηκε από τον FDA τον Σεπτέμβριο του 2019 και από τον EMA τον Ιανουάριο του 2020, για χρήση στον mHSPC σε συνδυασμό με ADT.
51